Lei de Segurança da Cadeia de Suprimentos de Medicamentos (DSCSA) sem embalagem
Desafios na rastreabilidade farmacêutica
O mercado farmacêutico dos EUA é responsável por mais de 40% das vendas globais de produtos farmacêuticos e espera-se que cresça de forma consistente nos próximos anos, atingindo mais de US$ 634 bilhões em 2024.ٟ Esse aumento é impulsionado por uma população crescente e envelhecida com maior renda disponível. Embora a grande maioria dos produtos farmacêuticos vendidos nos EUA seja segura, esse mercado grande e crescente é um alvo atraente para roubo e falsificação. Uma estimativa de longa data da Organização Mundial da Saúde (OMS) sugere que entre 5% e 8% dos produtos farmacêuticos vendidos no mundo todo são falsificados; muitos especialistas consideram essa estimativa baixa. Os produtos médicos falsificados podem conter os ingredientes ativos errados, nenhum ingrediente ativo ou ingredientes tóxicos, e geralmente são produzidos em condições insalubres por pessoal não treinado. Além disso, eles são cuidadosamente produzidos para parecerem idênticos aos produtos genuínos, o que dificulta sua detecção. Esses produtos fraudulentos podem não tratar a condição do paciente ou causar uma reação perigosa e possivelmente fatal. Houve inúmeros casos de alto nível em que produtos farmacêuticos ilegítimos causaram doenças e mortes. Para proteger os pacientes contra esses perigos, a segurança da cadeia de suprimentos de ciências da vida é essencial. Muitos países em todo o mundo já promulgaram e aplicaram requisitos de serialização e Track & Trace. A Drug Supply Chain Security Act (DSCSA) foi criada como uma ferramenta para ajudar a combater produtos farmacêuticos ilegítimos nos EUA.
Sobre a Lei de Segurança da Cadeia de Suprimentos de Medicamentos (DSCSA)
Promulgada em 2013, a DSCSA é uma lei federal dos EUA projetada para proteger a cadeia de valor das ciências da vida e proteger a segurança do paciente, fornecendo um padrão único para rastrear e acompanhar determinados medicamentos prescritos em toda a cadeia de suprimentos. A lei substitui uma série de exigências estaduais. Em resposta ao número crescente de produtos farmacêuticos abaixo do padrão ou falsificados, o sistema DSCSA verifica os produtos farmacêuticos em todos os estágios, desde o fabricante até o farmacêutico e o consumidor. Como a implementação em fases foi concluída em 2023, a rastreabilidade total em nível de unidade, incluindo a agregação, agora é necessária.
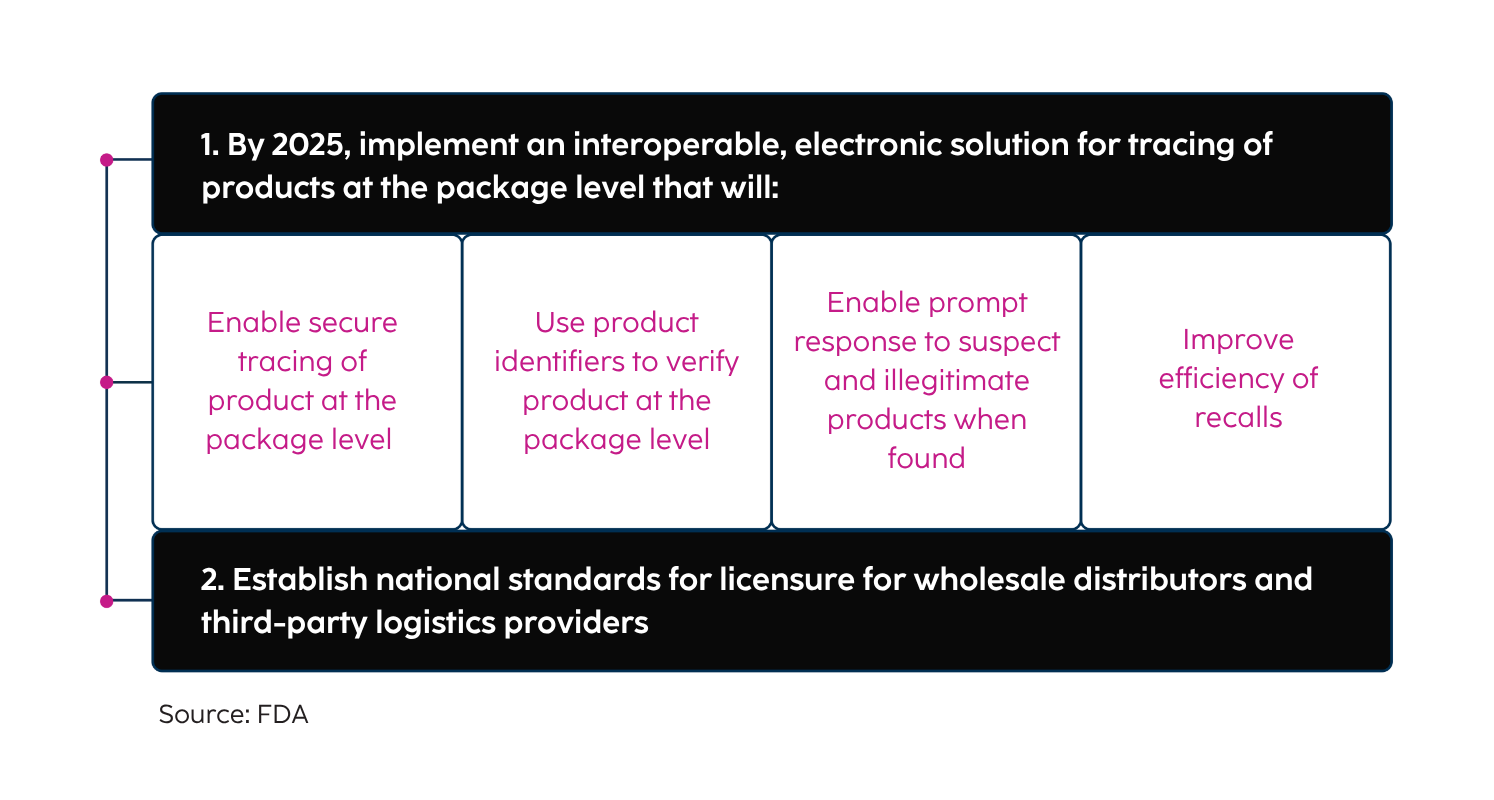
Metas da DSCSA
Benefícios da Lei de Segurança da Cadeia de Suprimentos de Medicamentos (DSCSA)
- Maior segurança para os pacientes, pois os medicamentos falsificados são impedidos de entrar na cadeia de suprimentos
- Maneiras novas e mais rápidas de identificar produtos ilegítimos na cadeia de suprimentos
- Cadeias de suprimentos mais seguras e eficientes
- Regulamentos mais claros com uma única fonte de verdade
- Padrões mais rígidos de licenciamento de distribuidores
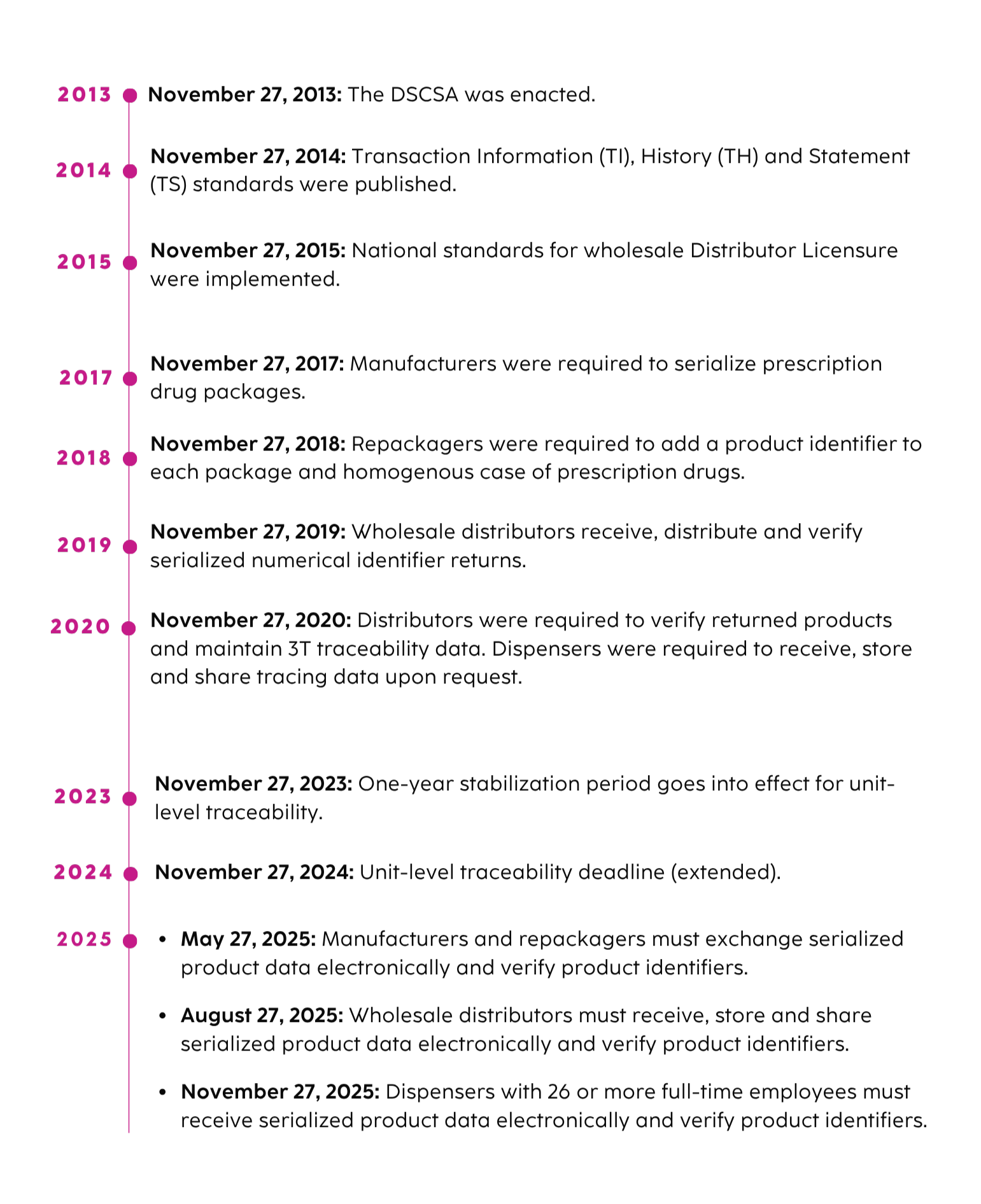
Marcos e cronograma de implementação da DSCSA
Requisitos da DSCSA
A DSCSA exige que os parceiros comerciais da cadeia de suprimentos farmacêutica - fabricantes, distribuidores atacadistas, reembaladores, empresas de logística terceirizadas e distribuidores (principalmente farmácias) - acompanhem, rastreiem e verifiquem os medicamentos prescritos, garantindo que somente os medicamentos adequados e seguros cheguem aos pacientes.
1. Identificação do produto
Os fabricantes e reembaladores são obrigados a serializar os produtos anexando um identificador de produto padronizado que inclui um identificador numérico padronizado (SNI) exclusivo para cada embalagem ou caixa, juntamente com o número do lote e a data de validade, todos apresentados em formatos legíveis por humanos e máquinas. Esses dados são incorporados a um código de matriz de dados bidimensional em cada embalagem e a um código de barras de matriz linear ou 2D em cada caixa homogênea. Além disso, os fabricantes e reembaladores devem manter registros desses identificadores de produtos por um período mínimo de seis anos.
2. Verificação do produto
Os fabricantes, distribuidores atacadistas de medicamentos, reembaladores e alguns distribuidores devem fornecer informações que verifiquem se um produto é legítimo e devem colocar em quarentena e investigar um produto que possa ser ilegítimo - em outras palavras, um produto suspeito de ser falsificado, desviado ou roubado. Deve haver um processo para notificar os parceiros comerciais e a FDA sobre produtos suspeitos de serem ilegítimos em tempo hábil, e um processo para responder a notificações de produtos ilegítimos.
3. Serialização de produtos
Os fabricantes devem serializar os medicamentos prescritos, incluindo o número de série, o número do lote, a data de validade e o identificador do produto (GTIN® ou NDC). Os fabricantes devem verificar os produtos no nível da embalagem e devem fornecer documentos 3T eletronicamente. Os reembaladores devem garantir a serialização dos medicamentos reembalados e devem ser capazes de gerar seus próprios números de série. Os reembaladores devem manter registros que associem os produtos originais às suas versões reembaladas. Eles só podem manusear determinados medicamentos prescritos se os produtos estiverem devidamente serializados e devem realizar a verificação no nível da embalagem.
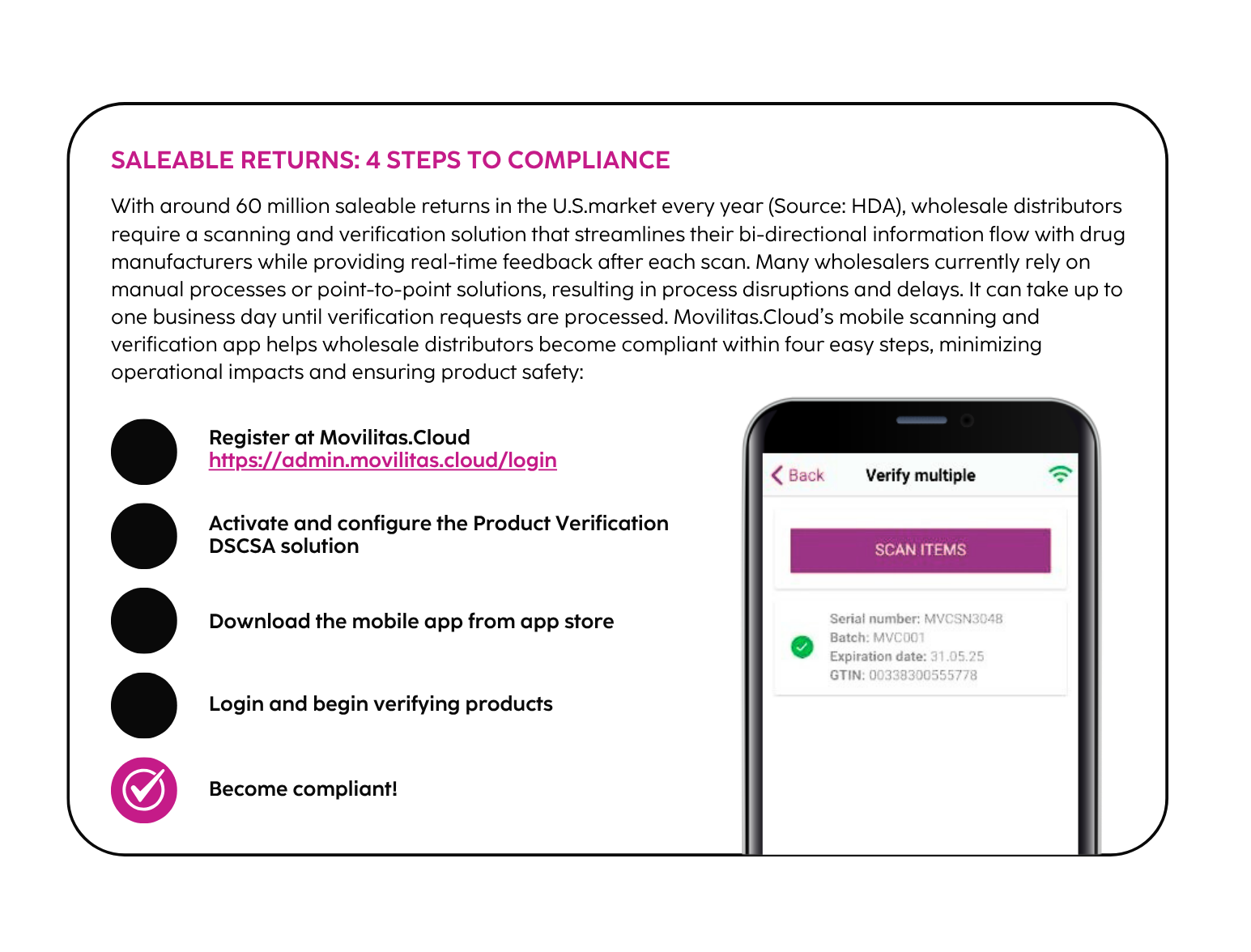
4. Devoluções vendáveis
Os distribuidores atacadistas devem verificar os identificadores de produtos serializados de todos os produtos farmacêuticos retornados vendáveis antes que eles possam ser revendidos. O atacadista inicia uma solicitação de verificação para o fabricante, que deve responder dentro de 24 horas com uma resposta de verificação. A verificação inclui a garantia de que o identificador do produto está correto e é verdadeiro, incluindo o número de série, o número do lote, a data de validade e o Número Global de Item Comercial (GTIN).
5. Parceiro comercial autorizado (ATP)
Como parte fundamental dos requisitos da DSCSA, os distribuidores e fabricantes de produtos farmacêuticos só devem se envolver com outros parceiros comerciais autorizados. A Movilitas.Cloud foi uma das primeiras a adotar essa iniciativa, provando ser um parceiro de soluções confiável para implementação e credenciamento rápidos.
6. Rastreamento de produtos
Os parceiros comerciais devem fornecer informações sobre um medicamento e quem o manipulou em cada transação no mercado farmacêutico dos EUA. Os fabricantes, distribuidores atacadistas e reembaladores, antes ou no momento da transação, devem fornecer aos parceiros comerciais informações sobre a transação, o histórico da transação e uma declaração da transação. Atualmente, os padrões de rastreamento de produtos exigem rastreabilidade no nível do lote, mas outras alterações entraram em vigor quando o DSCSA entrou na fase de EDDS (Enhanced Drug Distribution Security) em 2024, incluindo a exigência de rastrear produtos eletronicamente até o nível da embalagem.
Visão do Sistema Aprimorado de Distribuição de Medicamentos

O que você precisa fazer para estar em conformidade com a DSCSA
Como fabricante, distribuidor atacadista, reembalador, empresa de logística terceirizada ou distribuidor, você tem responsabilidades rigorosas para com seus clientes e outros parceiros comerciais, bem como requisitos de licenciamento e manutenção de registros e o dever de informar a FDA.
1. Negocie com parceiros devidamente licenciados
- Os fabricantes e reembaladores devem ter um registro válido na FDA.
- Os distribuidores e 3PLs devem ter licenças estaduais ou federais válidas e devem cumprir os requisitos de relatórios.
- Consulte o DECRS (Drug Establishment Current Registration Site) da FDA para verificar o licenciamento de seus parceiros comerciais.
2. Padronize os procedimentos operacionais para identificar produtos que possam ser falsificados
- Use o formulário FDA-3911 para notificar a FDA dentro de 24 horas se você acreditar que possui um produto ilegítimo.
- Notifique os parceiros comerciais em 24 horas.
- Coloque em quarentena e investigue os produtos que você acredita que possam ser ilegítimos.
- Tome medidas para garantir que os pacientes não recebam produtos ilegítimos.
3. Compartilhe os 3Ts durante todas as transações
- Informações sobre a transação (TI)
- Histórico de transações (TH)
- Extratos da transação (TS)
4. Rastreamento de produtos farmacêuticos
- Aceite somente produtos com informações completas de rastreamento, incluindo os 3Ts.
- Gere e forneça informações completas de rastreamento de produtos ao lidar com parceiros comerciais.
5. Prepare-se para responder às solicitações de informações
- Responda às solicitações dos parceiros comerciais em até dois dias úteis no caso de um recall ou outra investigação.
- Armazene as informações de rastreamento por pelo menos seis anos.
6. Verifique se há identificadores de produto adequados
- Um identificador de produto que contenha um NDC, número de série, número de lote e data de validade em formato legível por humanos e máquinas.
- Os fabricantes e reembaladores devem colocar um identificador de produto nas embalagens de medicamentos prescritos.
- Os distribuidores só podem comprar ou vender produtos farmacêuticos devidamente identificados e serializados.
Como podemos ajudar com o Movilitas.Cloud
Para estar em conformidade com a DSCSA e outras regulamentações farmacêuticas, as empresas devem implementar processos robustos de serialização e geração de relatórios que se conectem aos sistemas governamentais e aos parceiros da cadeia de suprimentos. Movilitas.Cloud, uma solução intuitiva e escalável de software como serviço (SaaS) da Engineering Industries eXcellence, ajuda a atender a esses requisitos. Seus aplicativos Serialized Manufacturing e Serialized Logistics otimizam a serialização de alto volume, garantem a integração de dados e oferecem suporte à conformidade de ponta a ponta em toda a cadeia de suprimentos.