La Ley de Seguridad de la Cadena de Suministro de Medicamentos (DSCSA) al descubierto
Retos de la trazabilidad farmacéutica
El mercado farmacéutico estadounidense representa más del 40% de las ventas mundiales de productos farmacéuticos y se espera que crezca de forma constante en los próximos años, hasta superar los 634.000 millones de dólares en 2024.ٟ Este aumento está impulsado por una población cada vez más envejecida y con mayor renta disponible. Aunque la gran mayoría de los productos farmacéuticos que se venden en Estados Unidos son seguros, este mercado grande y creciente es un objetivo atractivo para el robo y la falsificación. Una estimación realizada hace tiempo por la Organización Mundial de la Salud (OMS) sugiere que entre el cinco y el ocho por ciento de los productos farmacéuticos vendidos en todo el mundo son falsificados; muchos expertos consideran que esta estimación es baja. Los productos médicos falsificados o adulterados pueden contener principios activos erróneos, no contener principios activos o contener ingredientes tóxicos, y a menudo son fabricados en condiciones insalubres por personal sin formación. Además, se fabrican cuidadosamente para que parezcan idénticos a los productos auténticos, lo que dificulta su detección. Estos productos fraudulentos pueden fracasar en el tratamiento de un paciente o provocar una reacción peligrosa y posiblemente mortal. Ha habido numerosos casos muy sonados en los que productos farmacéuticos ilegítimos han causado enfermedades y muertes. Para proteger a los pacientes de estos peligros, la seguridad de la cadena de suministro de las ciencias de la vida es esencial. Muchos países de todo el mundo ya han promulgado y aplicado requisitos de serialización y seguimiento. La Ley de Seguridad de la Cadena de Suministro de Medicamentos (DSCSA) está diseñada como una herramienta para ayudar a combatir los productos farmacéuticos ilegítimos en los EE.UU.
Acerca de la Ley de Seguridad de la Cadena de Suministro de Medicamentos (DSCSA)
Promulgada en 2013, la DSCSA es una ley federal estadounidense diseñada para asegurar la cadena de valor de las ciencias de la vida y proteger la seguridad de los pacientes, proporcionando una norma única para el seguimiento y localización de determinados medicamentos con receta a lo largo de la cadena de suministro. La ley sustituye a una serie de requisitos estatales. En respuesta al creciente número de productos farmacéuticos de calidad inferior o falsificados, el sistema DSCSA verifica los productos farmacéuticos en todas las etapas, desde el fabricante hasta el farmacéutico y el consumidor. Una vez finalizada la implantación gradual en 2023, ahora se exige la trazabilidad completa a nivel unitario, incluida la agregación.
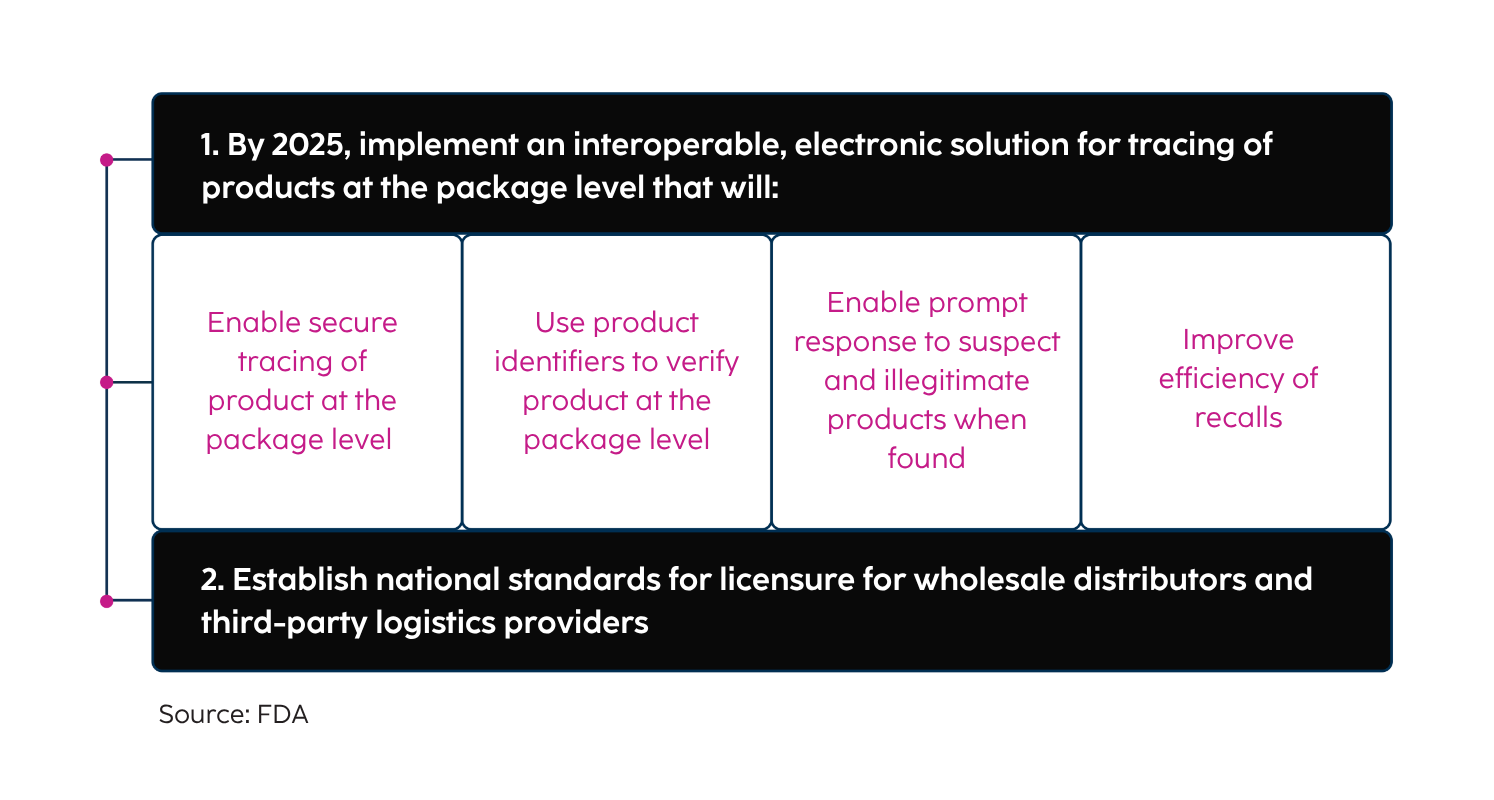
Objetivos de la DSCSA
Beneficios de la Ley de Seguridad de la Cadena de Suministro de Medicamentos (DSCSA)
- Mejora de la seguridad de los pacientes al impedir la entrada de medicamentos falsificados en la cadena de suministro
- Formas nuevas y más rápidas de identificar productos ilegítimos en la cadena de suministro
- Cadenas de suministro más seguras y eficientes
- Normativa más clara con una única fuente de información
- Normas más estrictas para la autorización de distribuidores
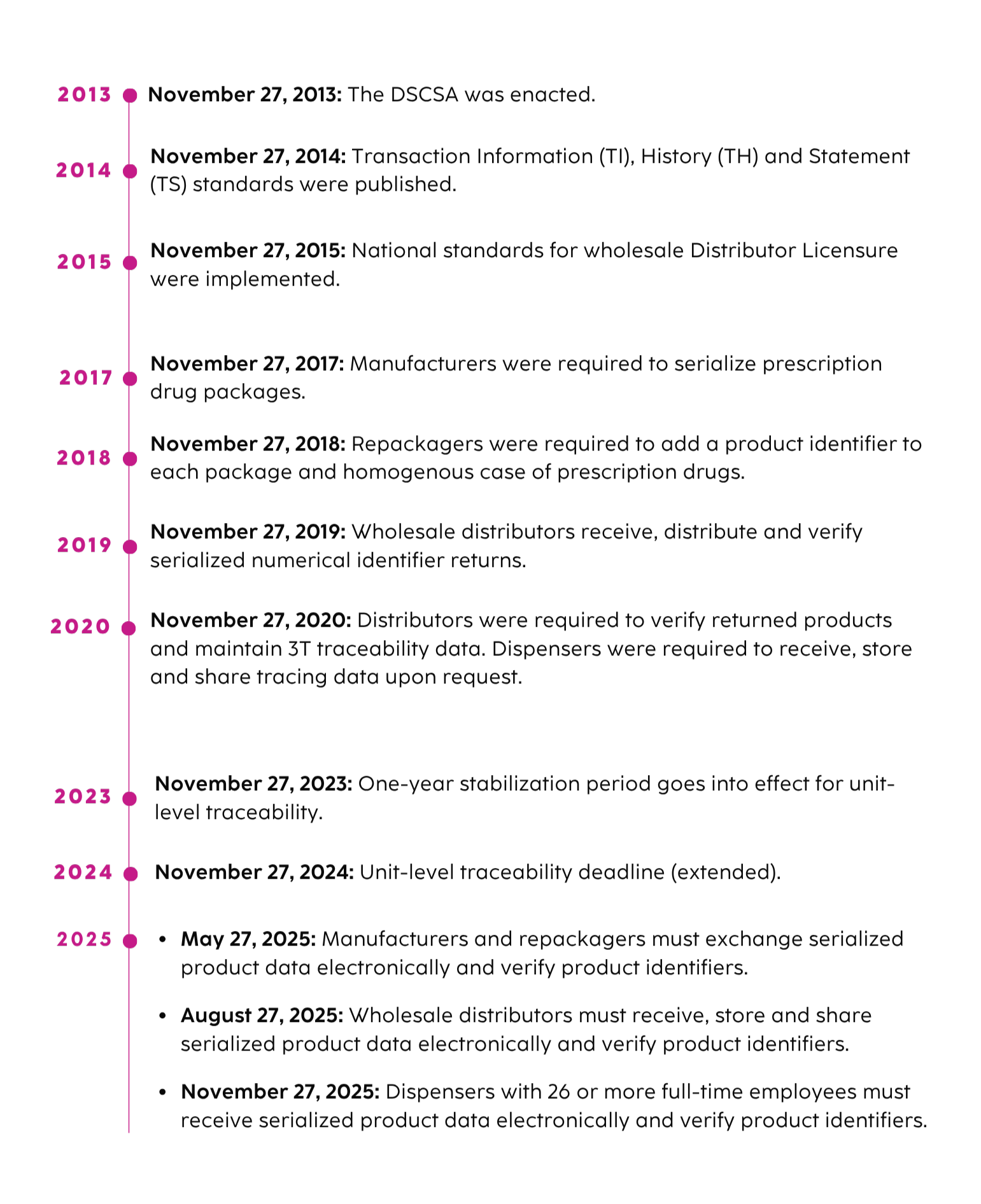
Hitos de la DSCSA y calendario de aplicación
Requisitos de la DSCSA
La DSCSA exige a los socios comerciales de la cadena de suministro farmacéutica -fabricantes, distribuidores mayoristas, reenvasadores, empresas logísticas externas y dispensadores (principalmente farmacias)- que realicen el seguimiento, la trazabilidad y la verificación de los medicamentos sujetos a receta médica, para garantizar que sólo los medicamentos adecuados y seguros lleguen a los pacientes.
1. 1. Identificación del producto
Los fabricantes y reenvasadores están obligados a serializar los productos adjuntando un identificador de producto normalizado que incluye un identificador numérico normalizado (SNI) único para cada envase o caja, junto con el número de lote y la fecha de caducidad, todo ello presentado en formatos legibles tanto por humanos como por máquinas. Estos datos se incluyen en un código de matriz de datos bidimensional en cada envase, y en un código de barras de matriz lineal o 2D en cada caja homogénea. Además, los fabricantes y reenvasadores deben mantener registros de estos identificadores de producto durante un mínimo de seis años.
2. Verificación del producto
Los fabricantes, distribuidores mayoristas de medicamentos, reenvasadores y algunos dispensadores deben proporcionar información que verifique que un producto es legítimo y deben poner en cuarentena e investigar un producto que pueda ser ilegítimo, es decir, un producto sospechoso de ser falsificado, desviado o robado. Debe existir un proceso para notificar oportunamente a los socios comerciales y a la FDA los productos sospechosos de ser ilegítimos, así como un proceso para responder a las notificaciones de productos ilegítimos.
3. Serialización de productos
Los fabricantes deben serializar los medicamentos con receta, incluyendo un número de serie, número de lote, fecha de caducidad e identificador del producto (GTIN® o NDC). Los fabricantes deben verificar los productos a nivel de envase y deben proporcionar los documentos 3T electrónicamente. Los reenvasadores deben garantizar la serialización de los medicamentos reenvasados y deben ser capaces de generar sus propios números de serie. Los reenvasadores deben mantener registros que relacionen los productos originales con sus versiones reenvasadas. Solo pueden manipular determinados medicamentos con receta si los productos están debidamente serializados y deben realizar la verificación a nivel de envase.
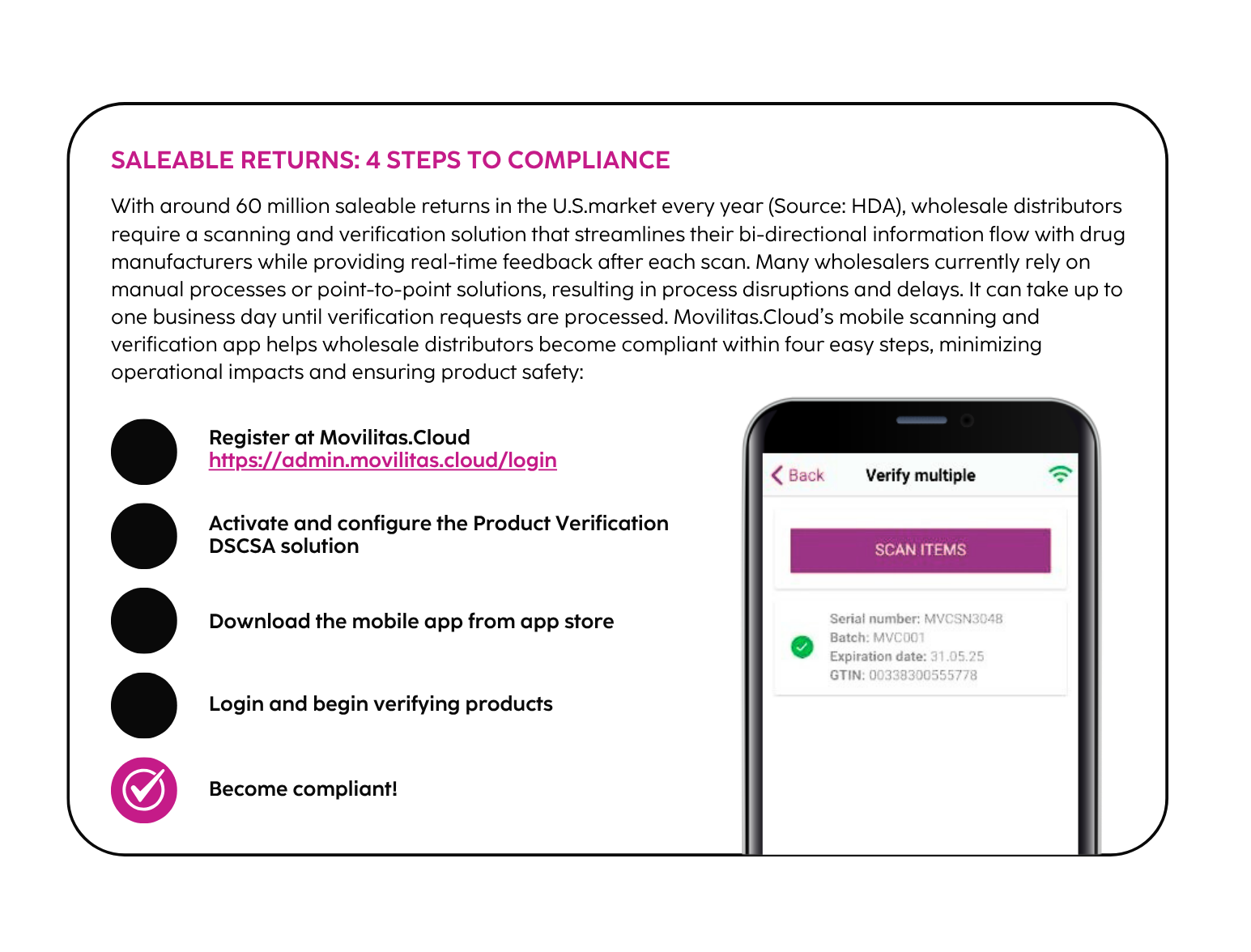
4. Devoluciones vendibles
Los distribuidores mayoristas deben verificar los identificadores de producto serializados de cualquier producto farmacéutico devuelto vendible antes de que pueda ser revendido. El mayorista inicia una solicitud de verificación al fabricante, que debe responder en un plazo de 24 horas con una respuesta de verificación. La verificación incluye asegurarse de que el identificador del producto es correcto y verdadero, incluidos el número de serie, el número de lote, la fecha de caducidad y el número de artículo de comercio mundial (GTIN).
5. Socio comercial autorizado (ATP)
Como parte fundamental de los requisitos de la DSCSA, los dispensadores, distribuidores y fabricantes de productos farmacéuticos solo deben relacionarse con otros socios comerciales autorizados. Movilitas.Cloud se convirtió en uno de los primeros en adoptar esta iniciativa, demostrando ser un socio de soluciones de confianza para una rápida implementación y acreditación.
6. Rastreo de productos
Los socios comerciales deben proporcionar información sobre un medicamento y quién lo ha manipulado en cada transacción en el mercado farmacéutico estadounidense. Los fabricantes, distribuidores mayoristas y reenvasadores, antes o en el momento de la transacción, deben proporcionar a los socios comerciales información sobre la transacción, el historial de transacciones y una declaración de la transacción. Actualmente, las normas de trazabilidad de productos exigen la trazabilidad a nivel de lote, pero se introdujeron cambios adicionales cuando la DSCSA entró en la fase de seguridad mejorada de la distribución de medicamentos (EDDS) en 2024, incluido el requisito de trazabilidad electrónica de los productos hasta el nivel de envase.
Visión del sistema mejorado de distribución de medicamentos

Qué debe hacer para cumplir la DSCSA
Como fabricante, distribuidor mayorista, reenvasador, empresa de logística de terceros o dispensador, tiene responsabilidades estrictas con sus clientes y otros socios comerciales, así como requisitos de licencia y mantenimiento de registros y la obligación de informar a la FDA.
1. 1. Comercie con socios debidamente autorizados
- Los fabricantes y reenvasadores deben tener un registro válido de la FDA.
- Los distribuidores y los 3PL deben tener licencias estatales o federales válidas y cumplir los requisitos de información.
- Consulte el Sitio de Registro Actual de Establecimientos Farmacéuticos (DECRS) de la FDA para verificar la licencia de sus socios comerciales.
2. Estandarice los procedimientos operativos para identificar productos que puedan estar falsificados
- Utilice el formulario FDA-3911 para notificar a la FDA en un plazo de 24 horas si cree que posee un producto ilegítimo.
- Notifíquelo a sus socios comerciales en un plazo de 24 horas.
- Ponga en cuarentena e investigue los productos que considere ilegítimos.
- Tome medidas para garantizar que los pacientes no reciban productos ilegítimos.
3. Comparta las 3T durante todas las transacciones
- Información de la transacción (IT)
- Historial de transacciones (TH)
- Extractos de las transacciones (TS)
4. Seguimiento y localización de productos farmacéuticos
- Sólo acepte productos con información de seguimiento completa, incluidas las 3T.
- Genere y proporcione información completa de rastreo de productos cuando trate con socios comerciales.
5. Prepárese para responder a las solicitudes de información
- Responda a las solicitudes de los socios comerciales en un plazo de dos días laborables en caso de retirada u otra investigación.
- Almacene la información de rastreo durante al menos seis años.
6. Compruebe que los identificadores de producto son correctos
- Un identificador de producto que contenga un NDC, número de serie, número de lote y fecha de caducidad en formato legible por humanos y máquinas.
- Los fabricantes y reenvasadores deben colocar un identificador de producto en los envases de los medicamentos con receta.
- Los dispensadores sólo pueden comprar o vender productos farmacéuticos debidamente identificados y serializados.
Cómo podemos ayudarle con Movilitas.Cloud
Para cumplir la DSCSA y otras normativas farmacéuticas, las empresas deben implantar procesos sólidos de serialización e información que conecten tanto con los sistemas gubernamentales como con los socios de la cadena de suministro. Movilitas.Cloud, una solución intuitiva y escalable de software como servicio (SaaS) de Engineering Industries eXcellence, ayuda a cumplir estos requisitos. Sus aplicaciones Serialized Manufacturing y Serialized Logistics agilizan la serialización de grandes volúmenes, garantizan la integración de datos y apoyan el cumplimiento de principio a fin en toda la cadena de suministro.