La legge sulla sicurezza della catena di approvvigionamento dei farmaci (DSCSA) è stata spiegata
Le sfide della tracciabilità farmaceutica
Il mercato farmaceutico statunitense rappresenta oltre il 40% delle vendite farmaceutiche globali e si prevede una crescita costante nei prossimi anni, fino a raggiungere oltre 634 miliardi di dollari nel 2024. Sebbene la stragrande maggioranza dei farmaci venduti negli Stati Uniti sia sicura, questo mercato ampio e in crescita è un bersaglio attraente per furti e contraffazioni. Secondo una stima di lunga data dell'Organizzazione Mondiale della Sanità (OMS), tra il cinque e l'otto per cento dei prodotti farmaceutici venduti nel mondo è contraffatto; molti esperti ritengono che questa stima sia bassa. I prodotti medici contraffatti o falsificati possono contenere ingredienti attivi sbagliati, nessun ingrediente attivo o ingredienti tossici, e sono spesso prodotti in condizioni igieniche precarie da personale non addestrato. Inoltre, sono prodotti con cura per sembrare identici ai prodotti originali, il che li rende difficili da individuare. Questi prodotti fraudolenti possono non curare la condizione del paziente o causare una reazione pericolosa e forse fatale. Ci sono stati numerosi casi di alto profilo in cui i prodotti farmaceutici illegali hanno causato malattie e morte. Per proteggere i pazienti da questi pericoli, la sicurezza della catena di approvvigionamento delle scienze della vita è essenziale. Molti Paesi in tutto il mondo hanno già adottato e applicato requisiti di serializzazione e tracciabilità. Il Drug Supply Chain Security Act (DSCSA) è stato concepito come strumento per aiutare a combattere i prodotti farmaceutici illegali negli Stati Uniti.
Informazioni sulla legge sulla sicurezza della catena di approvvigionamento dei farmaci (DSCSA)
Emanata nel 2013, la DSCSA è una legge federale statunitense progettata per rendere sicura la catena del valore delle scienze della vita e proteggere la sicurezza dei pazienti, fornendo un unico standard per la tracciabilità e la rintracciabilità di alcuni farmaci da prescrizione lungo tutta la catena di fornitura. La legge sostituisce una serie di requisiti statali. In risposta al crescente numero di prodotti farmaceutici scadenti o contraffatti, il sistema DSCSA verifica i farmaci in tutte le fasi, dal produttore al farmacista fino al consumatore. Con il completamento dell'implementazione graduale nel 2023, è ora richiesta la tracciabilità completa a livello di unità, compresa l'aggregazione.
Obiettivi del DSCSA
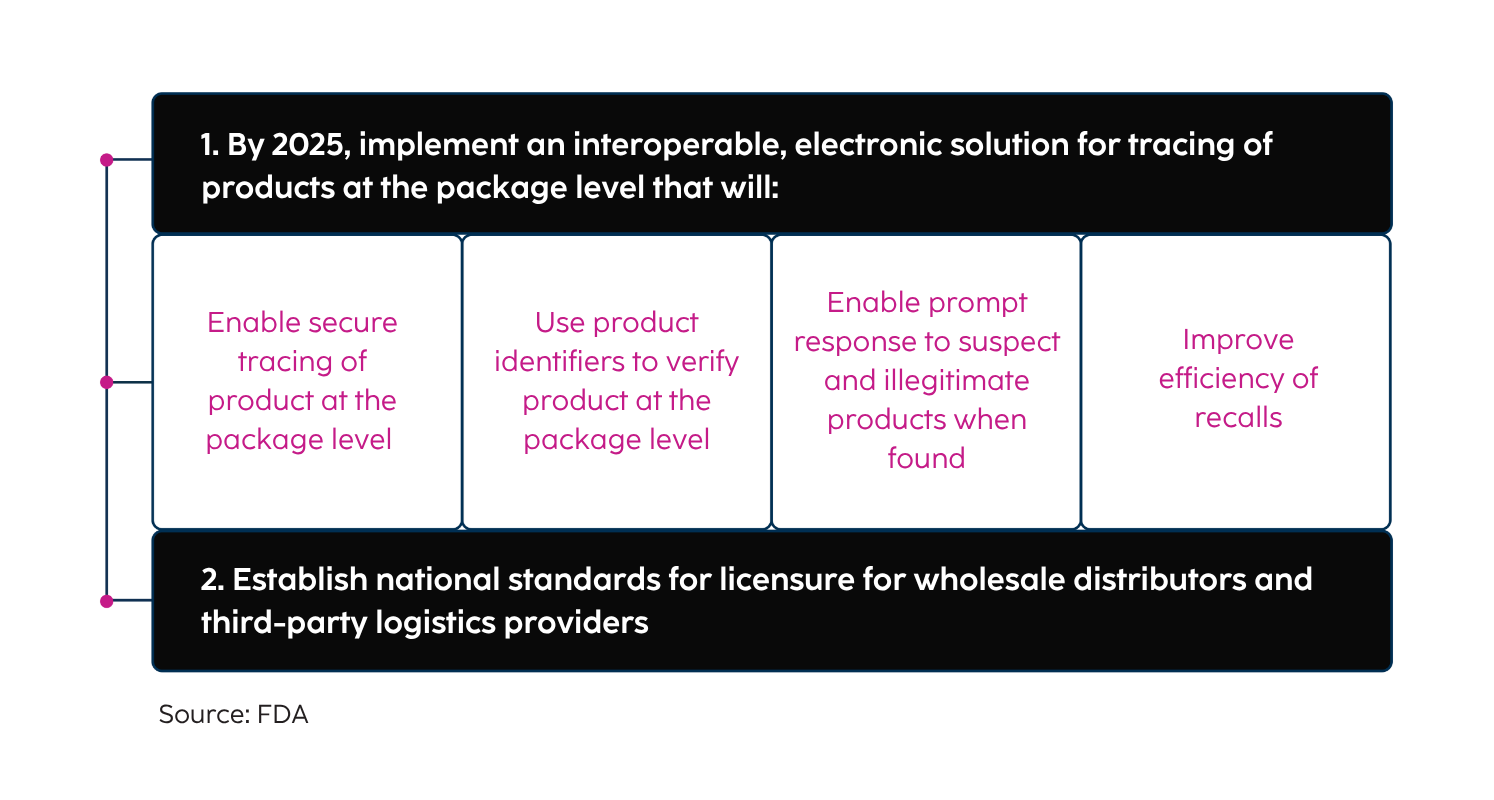
Benefici del Drug Supply Chain Security Act (DSCSA)
- Miglioramento della sicurezza dei pazienti grazie all'impossibilità di accedere alla catena di fornitura di farmaci contraffatti.
- Nuove e più rapide modalità di identificazione dei prodotti illegali nella catena di fornitura
- Catene di approvvigionamento più sicure ed efficienti
- Regolamenti più chiari con un'unica fonte di verità
- Standard più severi per la concessione di licenze ai distributori
Pietre miliari del DSCSA e tempistica di implementazione
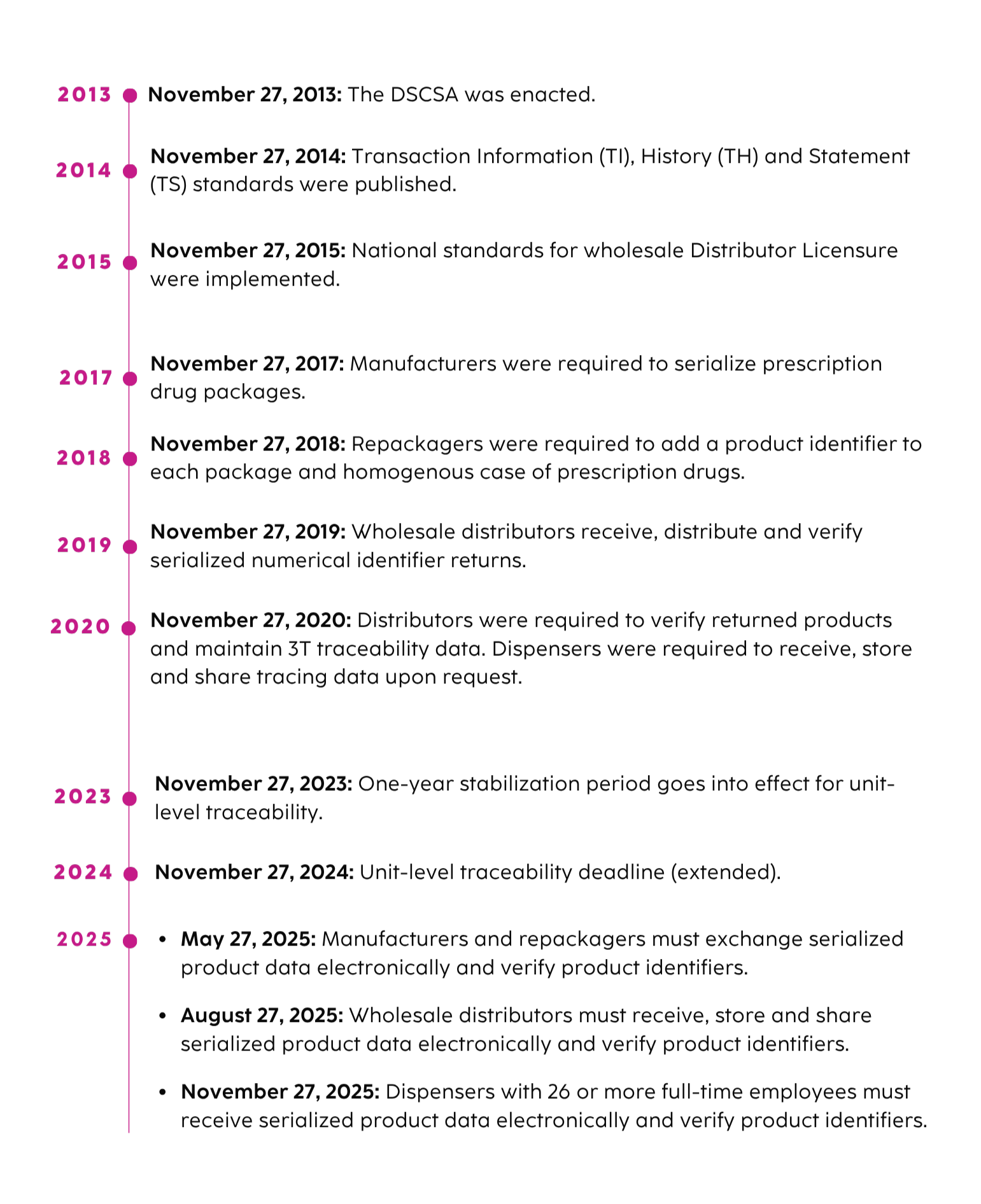
Requisiti del DSCSA
Il DSCSA richiede ai partner commerciali della catena di fornitura farmaceutica - produttori, distributori all'ingrosso, riconfezionatori, fornitori di logistica di terze parti e distributori (principalmente farmacie) - di tracciare, rintracciare e verificare i farmaci da prescrizione, assicurando che solo i farmaci appropriati e sicuri raggiungano i pazienti.
1. Identificazione del prodotto
I produttori e i riconfezionatori sono tenuti a serializzare i prodotti allegando un identificatore di prodotto standardizzato che comprende un identificatore numerico standardizzato (SNI) unico per ogni confezione o involucro, oltre al numero di lotto e alla data di scadenza, il tutto presentato in formati leggibili dall'uomo e dalla macchina. Questi dati sono incorporati in un codice a matrice di dati bidimensionale su ogni confezione e in un codice a barre lineare o a matrice 2D su ogni astuccio omogeneo. Inoltre, i produttori e i riconfezionatori devono conservare le registrazioni di questi identificatori di prodotto per un minimo di sei anni.
2. Verifica del prodotto
I produttori, i distributori all'ingrosso di farmaci, i riconfezionatori e alcuni distributori devono fornire informazioni che verifichino la legittimità di un prodotto e devono mettere in quarantena e indagare su un prodotto che potrebbe essere illegittimo - in altre parole, un prodotto sospettato di essere contraffatto, deviato o rubato. Deve esistere un processo per notificare tempestivamente ai partner commerciali e alla FDA i prodotti sospetti di essere illegittimi e un processo per rispondere alle notifiche di prodotti illegittimi.
3. Serializzazione dei prodotti
I produttori devono serializzare i farmaci da prescrizione, includendo un numero di serie, un numero di lotto, una data di scadenza e un identificativo del prodotto (GTIN® o NDC). I produttori devono verificare i prodotti a livello di confezione e devono fornire i documenti 3T in formato elettronico. I riconfezionatori devono garantire la serializzazione dei farmaci riconfezionati e devono essere in grado di generare i propri numeri di serie. I riconfezionatori sono tenuti a conservare i registri che collegano i prodotti originali alle loro versioni riconfezionate. Possono trattare alcuni farmaci da prescrizione solo se i prodotti sono adeguatamente serializzati e devono effettuare verifiche a livello di confezione.
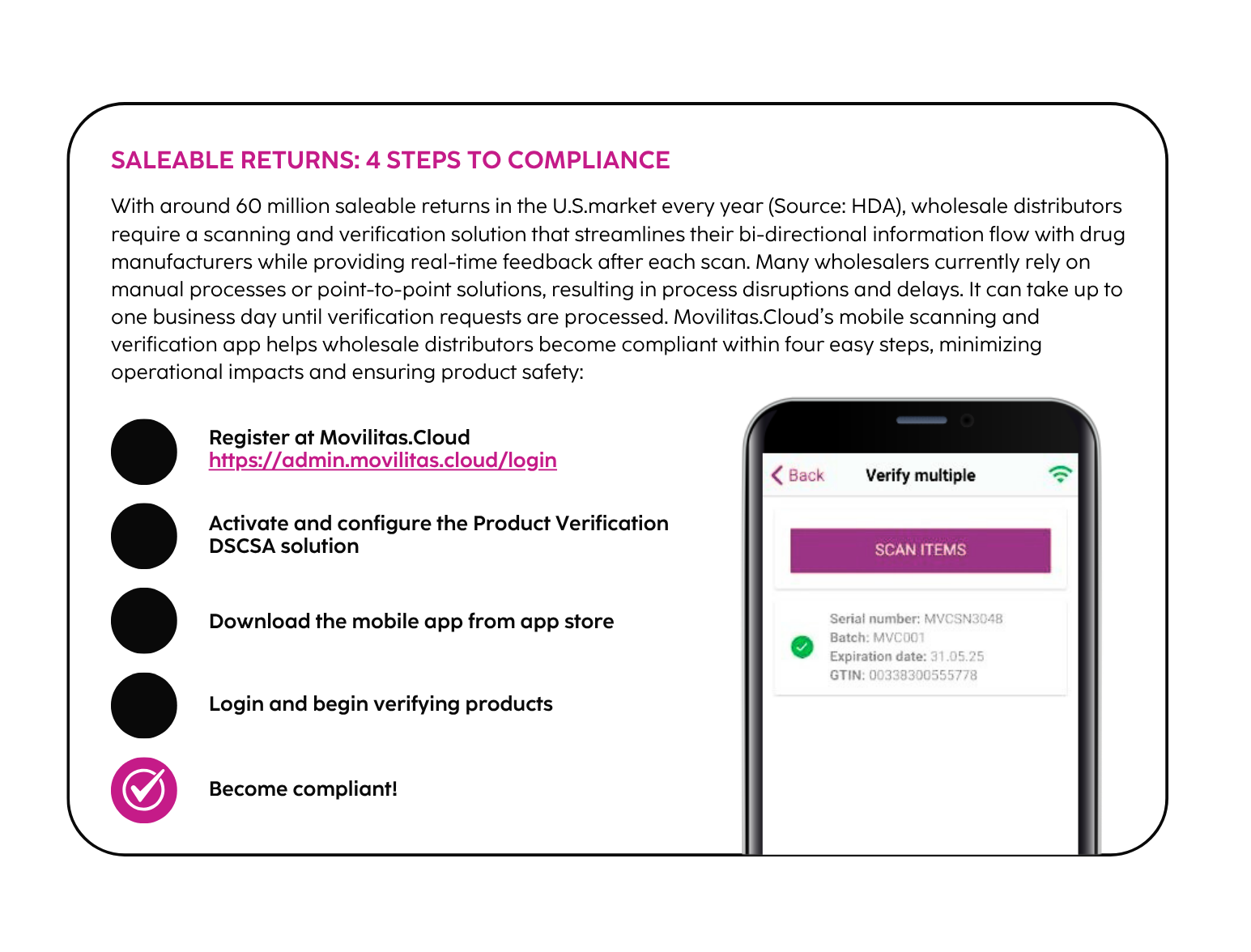
4. Resi vendibili
I distributori all'ingrosso devono verificare gli identificativi seriali dei prodotti farmaceutici resi vendibili prima di poterli rivendere. Il grossista avvia una richiesta di verifica al produttore, che deve rispondere entro 24 ore con una risposta di verifica. La verifica comprende la garanzia che l'identificativo del prodotto sia corretto e veritiero, compresi il numero di serie, il numero di lotto, la data di scadenza e il Global Trade Item Number (GTIN).
5. Partner commerciale autorizzato (ATP)
Come parte fondamentale dei requisiti del DSCSA, i dispensatori, i distributori e i produttori di farmaci devono impegnarsi solo con altri partner commerciali autorizzati. Movilitas.Cloud è stato uno dei primi ad adottare questa iniziativa, dimostrando di essere un partner affidabile per una rapida implementazione e credenziali.
6. Tracciabilità del prodotto
I partner commerciali devono fornire informazioni su un farmaco e su chi lo ha gestito per ogni transazione nel mercato farmaceutico statunitense. I produttori, i distributori all'ingrosso e i riconfezionatori, prima o al momento della transazione, devono fornire ai partner commerciali informazioni sulle transazioni, la cronologia delle transazioni e una dichiarazione delle transazioni. Gli standard di tracciabilità dei prodotti attualmente richiedono la tracciabilità a livello di lotto, ma ulteriori cambiamenti sono entrati in vigore quando il DSCSA è entrato nella fase di Enhanced Drug Distribution Security (EDDS) nel 2024, compreso l'obbligo di tracciare elettronicamente i prodotti fino al livello della confezione.
Visione del sistema potenziato di distribuzione dei farmaci

Cosa fare per conformarsi al DSCSA
In qualità di produttori, distributori all'ingrosso, riconfezionatori, aziende logistiche terze o dispensatori, avete responsabilità rigorose nei confronti dei vostri clienti e degli altri partner commerciali, nonché requisiti di licenza e di registrazione e l'obbligo di riferire all'FDA.
1. Commerciare con partner adeguatamente autorizzati
- I produttori e i riconfezionatori devono avere una registrazione FDA valida.
- I distributori e i 3PL devono essere in possesso di licenze statali o federali valide e devono rispettare i requisiti di rendicontazione.
- Controllate il Drug Establishment Current Registration Site (DECRS) della FDA per verificare la licenza dei vostri partner commerciali.
2. Standardizzare le procedure operative per identificare i prodotti che potrebbero essere falsificati
- Utilizzate il modulo FDA-3911 per notificare all'FDA entro 24 ore se ritenete di essere in possesso di un prodotto illegale.
- Informate i partner commerciali entro 24 ore.
- Mettere in quarantena e indagare sui prodotti che si ritiene possano essere illegittimi.
- Adottare misure per garantire che i pazienti non ricevano prodotti illegittimi.
3. Condividere le 3T durante tutte le transazioni
- Informazioni sulla transazione (TI)
- Storia della transazione (TH)
- Dichiarazioni di transazione (TS)
4. Tracciabilità dei prodotti farmaceutici
- Accettare solo prodotti con informazioni complete sulla tracciabilità, comprese le 3T.
- Generate e fornite informazioni complete sulla tracciabilità dei prodotti quando trattate con i partner commerciali.
5. Prepararsi a rispondere alle richieste di informazioni
- Rispondere alle richieste dei partner commerciali entro due giorni lavorativi in caso di richiamo o altre indagini.
- Conservare le informazioni di tracciabilità per almeno sei anni.
6. Verificare la presenza di identificatori di prodotto corretti
- Un identificativo del prodotto che contenga NDC, numero di serie, numero di lotto e data di scadenza in formato leggibile dall'uomo e dalla macchina.
- I produttori e i riconfezionatori devono apporre un identificatore di prodotto sulle confezioni dei farmaci da prescrizione.
- I distributori possono acquistare o vendere solo farmaci correttamente identificati e serializzati.
Come possiamo aiutarvi con Movilitas.Cloud
Per conformarsi al DSCSA e ad altre normative farmaceutiche, le aziende devono implementare solidi processi di serializzazione e reporting che si connettano sia con i sistemi governativi che con i partner della catena di fornitura. Movilitas.Cloud, una soluzione Software-as-a-Service (SaaS) intuitiva e scalabile di Engineering Industries eXcellence, aiuta a soddisfare questi requisiti. Le sue applicazioni di Serialized Manufacturing e Serialized Logistics ottimizzano la serializzazione di grandi volumi, assicurano l'integrazione dei dati e supportano la conformità end-to-end lungo tutta la catena di fornitura.